Министерство образования и науки Российской Федерации
Филиал федерального государственного бюджетного
образовательного учреждения
высшего образования
«Национальный исследовательский университет «МЭИ»
в г. Смоленске
Кафедра промышленной теплоэнергетики
Направление 13.03.01 Теплоэнергетика и теплотехника
профиль «Промышленная теплоэнергетика»
РЕФЕРАТ
по дисциплине «Физико-химические основы подготовки воды и топлива»
на тему
«Подготовка воды для систем горячего водоснабжения»
Cмоленск, 2015
ОГЛАВЛЕНИЕ
1. ВВЕДЕНИЕ
2. УМЯГЧЕНИЕ NA-КАТИОНИРОВАНИЕМ
3. ДЕКАРБОНИЗАЦИЯ
4. ФТОРИРОВАНИЕ И ОБЕСФТОРИВАНИЕ ВОДЫ
5. ДЕГАЗАЦИЯ ВОДЫ
6. ОБЕЗЖЕЛЕЗИВАНИЕ ВОДЫ
7. ОБЕЗЗАРАЖИВАНИЕ ВОДЫ
8. ЛИТЕРАТУРА
ВВЕДЕНИЕ
В настоящее время для обеспечения потребителей широко применяются системы централизованного теплоснабжения, которые подразделяются на:
· теплосети с открытым водоразбором (открытая теплосеть)
· закрытые теплосети с промежуточными теплообменниками, расположенными в абонентских районах.
В последние годы также получают распространение и децентрализованные, индивидуальные системы отопления и горячего водоснабжения.
Основными задачами водоподготовки и рациональной организации вводно-химического режима котлов, парогенераторов, тракта питательной воды и тепловых сетей являются:
· предотвращение образования на поверхностях нагрева котлов, теплообменников и других частей теплофикационных систем отложений накипи, окислов железа и т.п.,
· защита от коррозии конструкционных металлов основного и вспомогательного оборудования теплофикационных систем в условиях их контакта с водой и паром, а также при нахождении в резерве, длительном простое или на консервации.
Все вышеперечисленные мероприятия желательно проводить при минимальных капитальных затратах и с минимальными эксплуатационными расходами.
Требования по качеству подпиточной и сетевой воды устанавливаются в зависимости от типа теплосети:
1) Для теплосети с открытым водоразбором обработанная вода должна отвечать: требованиям для воды хозяйственно-питьевого назначения, качество которой регламентируется СанПИН 2.1.4.559-96., в частности ГОСТ «Вода питьевая». Величина общей жесткости не должна превышать 7 мг-экв/л, железа - 0,3 мг/л, значение щелочности pH 9,0.
2) Качество воды для закрытой сети определяется видом применяемого теплофикационного оборудования (котла, бойлера и т.п.). К качеству воды для закрытой сети в связи с отсутствием непосредственного водоразбора на нужды населения предъявляются менее строгие требования, основной задачей является обеспечение безнакипного режима работы применяемого теплофикационного оборудования (котлы, бойлера) и нормативно допустимого уровня коррозионной активности. Так, может быть допустимым повышение значения рН до 10,5 при одновременном глубоком умягчении, определяющим показателем является значение карбонатного индекса (И к), который в свою очередь определяет допустимый уровень накипеобразования - не выше 0,1.
Основным показателем безнакипного режима является величина карбонатного индекса - произведения общей щелочности на кальциевую жесткость, который имеет различные значения для данного температурного режима.
Обычно, основными нормативными документами, определяющими требования к качеству воды, являются:
- РД 24.031.120-91, РД10-165-97, РД10-179-98 – для параметров качества подпиточной воды
- СНиП II-35-76 «Котельные установки. Нормы проектирования»
- СНиП 2-04-07-86 «Тепловые сети»
- ПТЭ для электростанций и тепловых сетей РФ РД 34.20.501- 2002 и др.
Кроме этого, следует руководствоваться также рекомендациями производителей конкретного оборудования.
В последнее время с приходом на рынок зарубежных производителей, российских компаний активно занимающихся продвижением новых технологий и материалов для водоподготовки, наметилась тенденция для данных целей считать основными, современными способами подготовки воды, следующие:
- умягчение Na - катионированием с применением современных методов ионного обмена, с использование новых типов фильтрующих материалов и соответствующих им конструкций фильтров;
- декарбонизация воды с применением современных новых типов фильтрующих материалов (слабокислотных катионитов) и соответствующих им конструкций фильтров взамен Н - катионированием с «голодной» регенерацией
- очистка воды с применением мембранных технологий подготовки воды;
- применение программ химической обработки подпиточной воды с помощью дозирования современных более эффективных реагентов (ингибиторов коррозии, дисперсантов и ингибиторов солеотложения)
- также комбинирование всех вышеупомянутых методов
- альтернативные способы - в основном различные так называемые «преобразователи солей жёсткости» основанные на физических методах обработки воды.
УМЯГЧЕНИЕ NA-КАТИОНИРОВАНИЕМ
Сегодня метод одноступенчатого параллельно-точного Na - катионирования применяется наиболее широко. Данный процесс реализуется в фильтрах (различной конструкции и размеров в зависимости от производительности, требований к проведению самого процесса и т.п.). Сам ионообменный процесс происходит при фильтровании воды через слой ионообменной смолы (представляющей собой сильнокислотный катионит в Na-форме), загруженный в фильтр и периодически, по истощению, регенерируемый раствором поваренной соли. При этом происходит замена солей кальция (Ca2+), магния (Mg2+) на натрий (Na+) по следующей схеме:

Таким образом, вместо кальция (Ca2+), магния (Mg2+), вводится эквивалентное количество натрия (Na+). В результате получается умягченная вода, но при этом щелочность исходной воды практически не меняется в ходе обработки, а в случае ее повышенного значения вода будет обладать усиленными коррозионными свойствами вследствие разложения щелочности при нагреве. В качестве фильтрующих загрузок обычно служат сильнокислотные катиониты типа смолы КУ2-8 или сульфоуголь, регенерируемые поваренной солью.
Недостатками данного метода является:
- повышенный (обычно трехкратный) расход реагента (соли NaCl) по отношению к необходимому объему
- повышенный расход воды на собственные нужды
- повышенное содержание в сбросных водах хлоридов и натрия зачастую превышающих нормы.
- для получения глубоко умягчённой воды требуется вторая ступень
Современные способы ионирования и использование новых типов катионитов позволяют существенно оптимизировать процесс Na - катиониования – снизить расход реагентов на регенерацию, уменьшить расход воды на собственные нужды, сократить количество задействованного оборудования (фильтров). К таким методам относится противоточное катионирование, при котором поток фильтрата и регенерационного потока имеют противоположные направления. В частности, используется практически весь объем фильтра под загрузку катионита. Процент собственных нужд снижается до 3-4 %, расход соли уменьшается на 15-20 %. Появляется возможность получать фильтрат после первой ступени с качеством воды по жесткости не выше 10 –15 мкг-экв/л, то есть вторая ступень катионирования устраняется. Но стоит заметить, что данная технология требует высокой степени организации эксплуатации и желательна автоматизация технологических процессов.
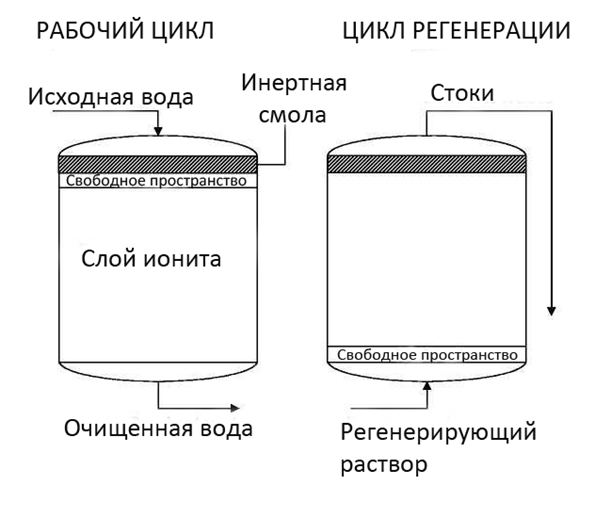
Рисунок 1. Схема выполнения противоточного ионирования по технологии UPCORE
Сегодня, кроме традиционно применяемых для умягчения в муниципальных котельных катионита КУ2-8 и сульфоугля, на рынке появились новые зарубежные материалы - более стабильные по качеству и поставляемые в Na-форме.
Особо следует отметить, что перевод катионита из одной формы в другую непосредственно у потребителя приводит не только к повышенным трудозатратам и дополнительному расходу воды и реагентов, но и зачастую приводит к снижению эксплуатационных показателей, в первую очередь, динамической обменной ёмкости. Объяснением этому служит сама процедура перевода из Н-формы в Na-форму, при которой вначале необходимо «истощить» катионит, слив кислую воду в канализацию (что приводит не только к загрязнению сточных вод, но и к коррозии трубопроводов), а только затем дважды отрегенерировать раствором поваренной соли перевести в Na-форму. Следует отметить также, что сильнокислотный катионит в Н-форме при пропускании через него исходной воды до «истощения» кроме солей жёсткости захватывает из неё и другие ионы, в том числе ионы металлов (железа, алюминия и т.д.), которые при последующей регенерации раствором поваренной соли не удаляются. Следовательно, часть функциональных групп заблокирована, в результате чего обменная емкость катионита после таких процедур снижается. Этих негативных процессов не происходит в случае применения для процессов умягчения воды специально, в заводских условиях, изготовленных катионитов в Na-форме.
Дальнейшим усовершенствованием противоточных процессов послужила разработка и поставка на рынок ионитов в виде моносфер, т.е. смол имеющих узкий фракционный эффективный состав гранул (количество частиц эффективного размера - около 05 - 0.6 мм достигает 95 %, тогда как у обычных ионитов оно составляет примерно 40 – 45 %).
Однако, неплохих результатов можно достигнуть, если применить катиониты и с обычным грансоставом (0.3-1.2 мм), но изготавливаемыми и поставляемыми потребителям в Na-форме. Для умягчения воды в котельной № 2 г. Нефтегорска был впервые применён сильнокислотный катионит Тульсион Т-42 в Na-форме, с фракционным составом 0.3-1.2 мм.
Катионит Тульсион Т-42 для процессов умягчения может поставляться сразу в Na-форме (в отличие от отечественных катионитов типа КУ2-8, обычно поставляемых в Н–форме), поэтому не требует трудоёмких и материалоёмких процессов по переводу из Н в Na- форму, т.к. эта процедура специальным образом выполняется во время производства катионита. Всё это позволяет производить фильтрование более эффективно и с более высокими скоростями.
Основные характеристики сильнокислотного катионита ТУЛСИОН Т- 42 приведены в табл.1
Таблица 1.
| Наименование | Характеристика |
| Характеристика | Высокоактивная гелевая смола |
| Тип | Сильнокислотный |
| Функциональная группа | Сульфоновая |
| Структура матрицы | Сополимер полистирола |
| Ионная форма | Na+/H+ |
| Внешний вид | Сферические зерна янтарного цвета |
| Размер частиц, мм | 0.3 - 1.2 |
| Общая обменная емкость, мг.экв/мл | 1.8 – Н + форма 2.0 – Na + форма |
| Влажность, % масс. | 45% Na+ форма 52% H+ форма |
| Диапазон рН | 0-14 |
| Растворимость | Нерастворима в обычных растворителях |
| Плотность, г/л | 830÷870 Na+ форма 800÷840 H+ форма |
ДЕКАРБОНИЗАЦИЯ
При подготовке подпиточной воды для систем ГВС, применяется также технология подготовки воды Н - катионированием с «голодной» регенерацией.
Технология Н-катионирования с «голодной» регенерацией позволяет существенно снизить карбонатную жесткость воды с частичным уменьшением некарбонатной. Все ионы водорода, вводимые в катионит с регенерационным раствором, полностью задерживаются, и вследствие этого в отработанных сточных водах кислота практически отсутствует. Расход регенерирующего реагента - серной кислоты является стехиометрическим, т.е. расчетным. Недостатками данного метода при использовании сульфоугля или КУ2-8 в Н-форме (отечественные специальные слабокислотные катиониты широкого распространения не получили) является пониженные эксплутационные характеристики, в частности:
· низкая скорость фильтрования (до 10 м/ч)
· низкая обменная емкость (200-250 г-экв /м3), как следствие
- большие затраты реагентов и воды на собственные нужды
-увеличенное количество фильтров
- трудность в управлении процессом (особенно в случае применения КУ2-8) и, как следствие, нестабильное качество воды
Сегодня, на рынке появились зарубежные слабокислотные катиониты, зачастую называемые карбоксильными катионитами которые специально созданы для удаления карбонатной жёсткости т.е. декарбонизации. К ним в частности относится слабокислотный катионит Тульсион СХО-12, от индийской компании «THERMAX Ltd».
При ионообменном способе декарбонизации воды на слабокислотном карбоксильном катионите к водородной форме (как наиболее экономичном) происходит замена солей кальция (Ca2+), магния (Mg2+) на водород (Н+) по следующей схеме:

Таким образом, вместо кальция (Ca2+), магния (Mg2+), вводится эквивалентное количество водорода (Н+). Далее анионы HCO3- взаимодействуют с образующимися катионами Н+ по реакции:
HCO3‑ + H+ - H2O + CO2 ↑
В результате происходит снижение концентрации бикарбонатов путём их «разрушения» и образование в результате углекислого газа. При этом, происходит снижение рН воды. Далее, для стабилизации рН воды требуется её отдувка на дегазаторе
Tulsion CXO – 12 MP высшего качества макропористый слабокислотный катионит на основе акрилат-ДВБ, поставляемый в Н-форме.
Tulsion CXO – 12 MP обладает превосходной физической и химической стабильностью, а также низкой набухаемостью гранул при ионных переходах.
Основные характеристики приведены в табл.2
Таблица 2
| 1. Тип 2. Матрица 3. Функциональная группа 4. Внешняя форма 5. Ионная форма при поставке 6. Размер гранул 7. Общая обменная ёмкость 8. Водоудержание 9. Набухание Н= -- Na = 10. макс. температура 11. Диапозон РН |
|
ФТОРИРОВАНИЕ И ОБЕСФТОРИВАНИЕ ВОДЫ
Содержание фтора в питьевой воде согласно СанПиН в зависимости от климатических условии должно поддерживаться в пределах 0,7—1,5 мг/л. Недостаток фтора в питьевой воде приводит к кариесу зубов у населения, а избыток к флюорозу.
В качестве фторсодержащих реагентов можно использовать: кремнефтористый натрий Na2SiF6, кремнефтористоводородную кислоту H2SiF6, фтористый натрий NaF, кремнефтористый аммоний (NH4)2SiF6, фтористый кальций CaF2, фтористоводородную кислоту HF, кремнефтористый калий K2SiF6, кремнефтористый алюминий Al2(SiF6)3, фтористый алюминий AlF3 и др. В отечественной практике широкое применение получил кремнефтористый натрий. Это мелкий, сыпучий, негигроскопический кристаллический порошок белого цвета, без запаха, удобен в эксплуатации. Плотность его 2,7 г/см3, рН насыщенного раствора 3,5—4,0. В воде растворяется плохо. Самый дешевый из всех перечисленных реагентов — фтористый кальций, но он имеет крайне низкую растворимость в воде (0,0016 г на 100 мл при 25°С).
Установки фторирования по технологии приготовления растворов фторсодержащих реагентов можно классифицировать: на установки сатураторного типа; с растворными баками (с механической мешалкой или с барботированием сжатым воздухом); с растворно-затворными баками; с применением кремнефтористоводородной кислоты.
На установках сатураторного типа в качестве реагента применяют порошкообразный кремнефтористый натрий, который вводят в воду перед хлорированием. Предварительно реагент замачивают и размешивают в емкости, а затем выливают в сатуратор (примерно 1 раз в смену). В основу работы сатуратора положен принцип объемного вытеснения.
Во фтораторных установках с растворными баками в качестве реагента используют кремнефтористый натрий. Для лучшего растворения реагента баки снабжены мешалками с частотой вращения 50—60 мин-1, возможно перемешивание сжатым воздухом. Время перемешивания 2 ч, время отстаивания 2 ч. Концентрация раствора реагента в баках оставляет 0,05 % по фтору или 0,008 % по чистой соли.
Фтораторные установки с затворно-растворными баками состоят из системы баков: затворного, двух растворных и дозирующего бака, снабженного поплавковым клапаном. Затворный и растворные баки оборудованы электро-смесителями. Растворяют фтористый натрий в воде, нагретой до 75—80 °С.
При применении 8%-ной кремнефтористоводородной кислоты она из автомобильной или железнодорожной цистерны, в которой транспортируется, с помощью воздуходувок передавливается в стационарные складские цистерны, а из них поступает в бак-мерник, откуда дозируется в воду.
В зарубежной практике фтористые соединения вводятся в воду в сухом виде -непосредственно порошком, сухими дозаторами, через растворную камеру или в жидком виде — дозаторами для растворов. Первый способ обычно реализуют на водоочистных комплексах большой производительности, второй — на установках малой производительности.
Для обесфторивания воды может быть использован ряд методов.
1. Метод сорбции фтора осадком гидроксида алюминия или магния, а также фосфата кальция, который целесообразно применять при обработке поверх-ностных вод, когда кроме обесфторивания требуется еще их осветление и обес-цвечивание. Вместе с тем метод используется для обработки подземных вод при необходимости одновременного умягчения воды реагентным методом (рис. 2).
Исследования, выполненные в МГСУ (Г.И. Николадзе и др.), показали, что процесс сорбции фтора свежеобразованным гидроксидом магния при рН = 9 протекает быстро и интенсивно, практически не зависит от температуры и заканчивается за 8—12 мин, сорбционная способность гидроксида магния может быть использована более полно пропусканием обрабатываемой воды через его взвешенный слой.
Рекомендуемая скорость восходящего движения воды в осветлителях от 0,2 до 0,3 мм/с. Высота слоя осадка принимается 2 - 2,5 м. Время пребывания воды в слое контактного осадка не менее 1 ч. При этом расход магния на удаление 1 мг фтора - около 30 мг.
Обесфторивание воды солями алюминия целесообразно проводить при низких значениях рН = 4,3 - 5. В этом случае в осадке преимущественно находится основной сульфат алюминия — A1(OH)SO4 и уменьшается содержание гидроксида алюминия А1(ОН)3 который сорбирует фтор в меньшей степени, чем
Al(OH)SO4. При таких рН требуются меньшие дозы сульфата алюминия: 25—30 мг на 1 мг удаляемого фтора.
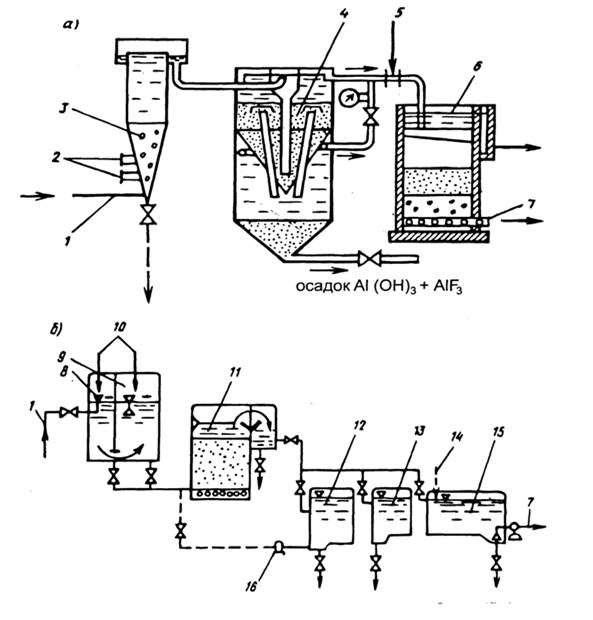
Рисунок 2. Схема дефторирования воды сорбцией на свежеобразованном гидроксиде алюминия (а) и фильтрованием через зернистую загрузку, заряженную сульфат-ионами (б):
1, 7 - подача исходной и отвод дефторированной воды; 2 — ввод раствора извести (соды) и сульфата алюминия; 3 — смеситель; 4 осветлитель со слоем взвешенного осадка; 5 — ввод кислоты для стабилизации воды; 6 — скорый фильтр; 8, 9 — зарядная и рабочая камеры смесителя; 10 - подача сульфата алюминия; 11 – контактный осветлитель; 12 — резервуар сбора первого фильтрата; 13 — отстойник промывной воды; 14 — ввод хлора; 15 — резервуар чистой воды; 16 – насос.
Удаление фтора из воды с помощью трикальцийфосфата основано на сорбции свежеобразованным трикальцийфосфатом, который связывает имеющийся в воде фтор в малорастворимое соединение — [Са9 (PO4)6Ca]F2, выпадающее в осадок. Расход трикальцийфосфата на удаление 1 мг фтора составляет 23—30 мг. Связывание фтора описывается следующей реакцией:
ЗСа3 (РO4)2 + NaF + Са(НСO3)2 → [Са9 (PO4)6Ca]F2 + 2NaHCO3.
Скорость восходящего потока воды в слое взвешенного осадка принимают 0,6—0,8 мм/с. Содержание фтора снижается с 5 до 1 мг/л при расходе реагента 30 мг на 1 мг удаленного фтора.
2. B.Л. Драгинский (НИИ КВОВ) и др. предложили обесфторивание воды методом контактно-сорбционной коагуляции. Коагулянт — сернокислый алюминий вводится в воду непосредственно перед контактными осветлителями. Метод применим при концентрации фтора до 5 мг/л, сероводорода до 2 мг/л, щелочности до 6 мг-экв/л. На 1 мг удаляемого фтора расходуется около 80 мг сульфата алюминия.
3. Дефторирование воды активированным оксидом алюминия (дефлюоритом) обеспечивает высокий эффект удаления фтора из подземных вод. Зернистый активированный оксид алюминия (ЗАОА) является наиболее дешевым сорбентом, простым в изготовлении и емким по поглощению фтора. При фильтровании обрабатываемой воды со скоростью 5—7 м/ч через ЗАОА происходит поглощение фтора сорбентом в результате обмена сульфат-ионов на фтор-ионы. Регенерация сорбента производится пропуском через него 1—1,5 % - ного раствора сульфата алюминия. Емкость поглощения 1 г ЗАОА составляет 2—2,5 мг фтор-ионов.
Обесфторивание воды по данному методу характеризуется наибольшим технико-экономическим эффектом, так как себестоимость обработки воды здесь минимальная по сравнению со всеми ранее рассмотренными методами.
4. Для подземных вод, не требующих осветления и обесцвечивания, возможно обесфторивание с применением сильноосновных анионитов. По экономическим соображениям это целесообразно при необходимости одновременного опреснения воды.
ДЕГАЗАЦИЯ ВОДЫ
Дегазация воды — комплекс мероприятий, связанных с удалением из воды растворенных в ней газов. Различают физические (безреагентные), химические (реагентные) и комбинированные (биохимические, электрохимические, физико-химичес- кие) способы.
Физические способы дегазации воды — это ее аэрация, пенная дегазация, кипячение, вакуумирование.
Химические способы дегазации воды — это добавление в нее химических реагентов, вступающих в реакцию с растворенным в воде газом, в результате чего происходят связывание или окисление удаляемого газа и перевод его в менее активные соединения с последующим удалением из воды.
Комбинированные способы дегазации воды предусматривают совместное использование физических и химических методов, иногда с привлечением некоторых дополнительных факторов (микроорганизмов, электрического тока и др.)
Физическими методами обычно удаляются СO2, H2S, а O2 удаляют химическим путем.
Аэрирование воды производится в специальных установках вакуумно-эжекционного, пенного, пленочного типов, а также используются брызгальные бассейны, аэраторы каскадного типа.
Одним из наиболее совершенных аэраторов является дегазатор пленочного типа (рис. 3), загруженный керамическими или пластмассовыми кольцами для увеличения поверхности контакта аэрируемой воды и воздуха. Обрабатываемая вода стекает тонкой пленкой сверху вниз, а снизу под контактную массу вентилятором нагнетается воздух.
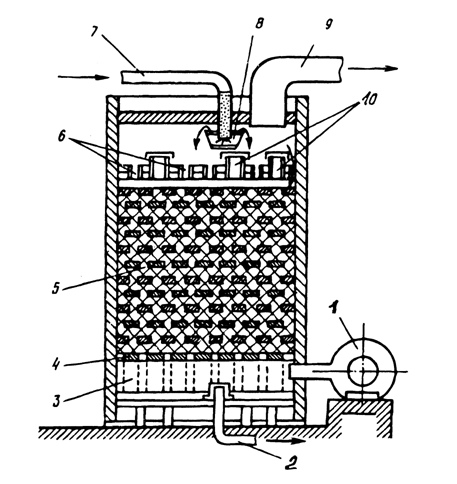
Рисунок 3. Аэрационный аппарат пленочного типа:
1 — вентилятор; 2 — отвод дегазированной воды; 3 — поддон; 4 — дренажная плита; 5 — насадка из кольца Рашига или пластмассовых колец; 6 —оросительные патрубки; 7— подача исходной воды; 8 — распределительная чаша; 9 — отвод выделившихся газов; 10 — патрубки отвода газовой смеси.
Площадь поперечного сечения дегазатора, загруженного кольцами Рашига, принимается исходя из удельного расхода воды 60 м3/(м2 ∙ ч). Удельный расход воздуха составляет 15 м3/(м2 ∙ ч).
H2S, O2 и СO2 удаляются также химическими методами при введении реагентов или фильтрованием через специальные загрузки.
O2 может удаляться фильтрованием через легко окисляющиеся вещества (стальные стружки), или при взаимодействии с сульфитом натрия Na2SO3, или оксидом серы S02, или, в редких случаях, при применении гидразина N2H4.
Для удаления сероводорода из воды химическими методами его окисляют кислородом воздуха, или хлором С12, или двухлора С120, или перманганатом калия КМп04, или озоном 03. Также можно использовать взаимодействие H2S с гидроокисью железа (III) Fe(OH)3. Сероводород может окисляться серобактериями до серы.
Углекислый газ СO2 химическим путем связывается известью в практически нерастворимый карбонат кальция СаСO3.
Тот или иной способ и технологию дегазации воды выбирают на основании технико-экономических расчетов и с учетом местных конкретных условий объекта водоснабжения.
ОБЕЗЖЕЛЕЗИВАНИЕ ВОДЫ
Железо в природных водах может содержаться в виде двухвалентного железа, неорганических и органических коллоидов, а также в форме комплексных соединений двух и трехвалентного железа или тонкодисперсной взвеси гидрата окиси железа.
Обезжелезивание воды для хозяйственно-питьевых целей производится при содержании в ней железа более 0,3 мг/л. Многообразие форм и концентраций железа, встречающихся в природных водах, вызвало необходимость разработки ряда методов, технологических схем и сооружений обезжелезивания воды. Все методы обезжелезивания можно свести к двум основным типам: безреагентные и реагентные.
Обезжелезивание поверхностных вод можно осуществить лишь реагентными методами, а для удаления железа из подземных вод наибольшее распространение получили безреагентные методы.
Из используемых безреагентных методов обезжелезивания воды перспектив-ными являются: вакуумно-эжекционная аэрация и фильтрование; упрощенная аэрация и фильтрование; «сухая» фильтрация; фильтрование на каркасных фильтрах; фильтрование в подземных условиях с предварительной подачей в пласт оксидированной воды или воздуха; аэрация и двухступенчатое фильтрование.
К реагентным относят следующие методы: упрощенная аэрация, оксидация, фильтрование; напорная флотация с известкованием и последующим фильтрованием; известкование, отстаивание в тонкослойном отстойнике и фильтрование; фильтрование через модифицированную загрузку; электро-коагуляция; катионирование.
Безреагентные методы обезжелезивания могут быть применены, когда исходная вода характеризуется: рН — не менее 6,6; щелочность — не менее 1,5 мг-экв/л; содержание углекислоты — до 80 мг/л и сероводорода — до 2 мг/л; перманганатная окисляемость — не более 9,5 мг О2/л. При соблюдении этих условий при содержании железа (III) не более 10 % общего и концентрации железа (II) в бикарбонатной или карбонатной форме до 3 мг/л рекомендуется метод фильтрования на каркасных фильтрах без вспомогательных фильтрующих средств; до 5 мг/л — предпочтительно применять метод «сухой» фильтрации; от 5 до 10 мг/л — следует использовать метод упрощенной аэрации с одноступенчатым фильтрованием; от 10 до 20 мг/л — аэрация и двухступенчатое фильтрование; от 10 до 30 мг/л — рекомендуется вакуумно- эжекционная аэрация с фильтрованием через загрузку большой грязеемкости. При содержании углекислого или карбонатного железа (II) более 20 мг/л или при наличии сероводорода 1—5 мг/л и рН не ниже 6,4 рекомендуется метод вакуумно-эжекционной аэрации с последующим отстаиванием в тонком слое воды или обработкой в слое взвешенного осадка и фильтрование.
Реагентные методы обезжелезивания воды применяют при низких значениях рН, высокой окисляемости, нестабильности воды. При этом при содержании сернокислого или карбонатного железа либо комплексных железоорганических соединений до 10 мг/л и перманганатной окисляемости до 15 мг O2/л рекомендуется применять фильтрование через модифицированную загрузку; до 15 мг/л и перманганатной окисляемости до 15 мг O2/л предпочтителен метод, предусматривающий упрощенную аэрацию, обработку сильным окислителем и фильтрование через зернистую загрузку большой грязеемкости; свыше 10 мг/л и перманганатной окисляемости более 15 мг O2/л следует применять напорную флотацию с предварительным известкованием и последующим фильтрованием или метод, предусматривающий аэрацию, известкование, отстаивание в тонком слое и фильтрование; свыше 10 мг/л, перманганатной окисляемости более 15 мг O2/л при производительности установок до 200 м3/сут можно рекомендовать электрокоагуляцию с барботированием, отстаиванием в тонком слое и фильтрование. Обезжелезивание воды катионированием целесообразно лишь в тех случаях, когда одновременно с обезжелезиванием требуется умягчение воды, при этом ионным обменом могут быть извлечены только ионы железа (II).
ОБЕЗЗАРАЖИВАНИЕ ВОДЫ
На заключительном этапе очистки воды для хозяйственно-питьевых нужд производится ее обеззараживание, так как приосветлении и обесцвечивании природной воды в ней еще остаются 5—10 % бактерий, среди которых могут оказаться и патогенные бактерии и вирусы. Использование подземной воды в большинстве случаев возможно без обеззараживания. В технологии водоподготовки известен ряд методов обеззараживания: термический, химический, олигодинамия (с помощью благородных металлов), физический (с помощью ультразвука, радиоактивного излучения, ультрафиолетовых лучей). Наиболее широко используется химический способ, предусматривающий применение сильных окислителей: хлора и его производных, озона, перекиси водорода, магранцевокислого калия, гипохлорита натрия и кальция. На практике предпочитают использовать хлор, хлорную известь, гипохлорит натрия, озон.
Выбор метода зависит от расхода и качества обрабатываемой воды, эффективности ее очистки, условий поставки и хранения реагентов, возможности автоматизации и механизации трудоемких работ.
Хлорирование воды является надежным санитарно-гигиеническим приемом предотвращения распространения эпидемий, так как большинство патогенных бактерий (бациллы брюшного тифа, туберкулеза и дизентерии, вибрионы холеры, вирусы полиомиелита и энцефалита и др.) весьма нестойки по отношению к хлору. Спорообразующих бактерий хлор не уничтожает, что является одним из недостатков этого метода обеззараживания.
Дозу активного хлора для обеззараживания устанавливают на основании данных технологических изысканий. При их отсутствии для предварительных расчетов дозу принимают для поверхностных вод после фильтрования 2—3 мг/л, для подземных — 0,7—1,0 мг/л.
Хлорсодержащие реагенты вводят в трубопровод фильтрованной воды, а для подземных вод, не требующих очистки, — перед резервуарами чистой воды. Концентрация остаточного свободного хлора в воде, забираемой из резервуара чистой воды, должна быть в пределах 0,3-0,5 мг/л, а связанного хлора — 0,8—1,2 мг/л при минимальной продолжительности контакта соответственно 30 и 60 мин. Для качественного хлорирования необходимо также хорошее перемешивание.
Хлорирование воды осуществляют жидким (газообразным) хлором. На водоочистных комплексах с расходом до 3000 м3/сут допускается применение хлорной извести.
При плюсовых температурах и атмосферном давлении хлор представляет собой газ зеленовато-желтого цвета с удушливым запахом и плотностью, значительно большей, чем плотность воздуха. При повышении давления хлор переходит в жидкое состояние, в таком виде его перевозят и хранят в специальных стальных емкостях (при давлении 0,6—1,0 МПа). Хлор поставляется в баллонах двух типов вместимостью до 25—30 кг и 100 кг жидкого хлора. На крупные водоочистные комплексы производительностью более 100 тыс. м3/сут хлор доставляют обычно в железнодорожных цистернах вместимостью до 48 т жидкого хлора, а хранят его в бочках, которые в зависимости от размеров вмещают от 700 до 3000 кг жидкого хлора. Хлорное хозяйство должно обеспечивать прием, хранение, испарение жидкого хлора, дозирование газообразного хлора с получением хлорной воды.
Гидролиз хлора происходит по реакции:
Сl2 + Н2O ↔ НС1 + НОС1.
Хлорноватистая кислота диссоциирует с образованием гипохлоритного иона (ОС1-), при этом оксидирующее воздействие на микроорганизмы оказывают как сама хлорноватистая кислота, так и главным образом гипохлоритный ион. Степень диссоциации хлорноватистой кислоты зависит от рН. При использовании вместо хлора хлорной извести протекает реакция
2СаОС12 + 2Н2O ↔ СаС12 + Са (ОН) 2 + 2НОС1.
Доза вводимого хлора должна быть больше величины хлоропоглощаемости на величину остаточного хлора, присутствие которого является гарантией того, что оксидация бактерий и органических веществ в воде практически завершена.
На практике в зависимости от качества исходной воды делают предварительное хлорирование, вводя хлор перед смесителями дозой 5 мг/л, что способствует оксидации органических защитных коллоидов, препятствующих коагуляции, а также гуминовых веществ, обусловливающих цветность. При этом улучшается санитарное состояние очистных сооружений, снижается общий расход хлора.
Для обеспечения более длительного бактерицидного действия хлора и предотвращения появления в воде хлорфенольных запахов и привкусов применяют предварительную аммонизацию, т. е. вводят аммиак в воду раньше хлора. При этом образуются монохлорамины:
HCl + NH3 ↔ NH2C1 + Н2O,
которые, гидролизуясь, образуют гипохлоритный ион:
NH2C1 + H20 → NH4+ + ОС1-.
Гидролиз хлораминов протекает медленно, и длительность бактерицидного действия увеличивается, хотя окисляющая способность хлораминов ниже, чем хлора.
Аммиак хранят на расходном складе в баллонах или контейнерах. Ввод аммиака производят в фильтрат, при наличии фенолов — за 2—3 мин до ввода хлора.
Для ввода в воду хлора, аммиака и сернистого газа (при дехлорировании) применяют вакуумные газодозаторы системы ЛОНИИ-100 (рис.4) и системы JI.A. Кульского. Из исходных баллонов жидкий хлор перетекает в промежуточный баллон, где происходит его испарение и отделение загрязнений. Далее газообразный хлор проходит через фильтр со стекловатой и затем через понижающий давление редуктор. Степень понижения давления фиксируется двумя манометрами, установленными до и после редукционного клапана. С помощью диафрагмы создается перепад давления, который служит импульсом для работы измерителя расхода хлора. Затем хлор поступает в смеситель, смешивается с водопроводной водой, образуя хлорную воду, которая подсасывается эжектором и таким образом дозируется в обрабатываемую воду.
С одного стандартного баллона при комнатной температуре можно получить не более 0,5—0,7 кг хлоргаза. Для увеличения съема хлора прибегают к специальному обогреву баллонов теплой водой или подогретым воздухом при температуре 10—30 °С.
Дехлорирование воды, т. е. удаление при необходимости избытка остаточного хлора, можно осуществлять при небольшом избытке — аэрированием, при большом — химическими методами (обработка воды гипосульфитом или сульфитом натрия, аммиаком), фильтрацией через активированный или сульфоуголь.
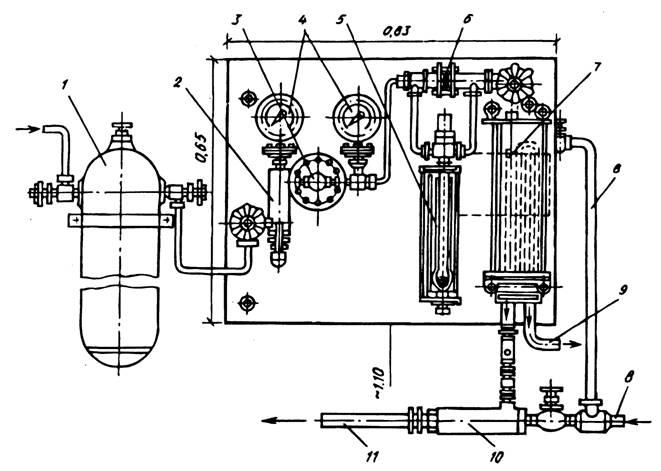
Рисунок 4. Хлоратор ЛОНИИ-100:
7 — промежуточный баллон с хлором; 2 — фильтр со стекловатой; 3 — редукционный клапан для снижения давления хлоргаза; 4 — манометры; 5 — ротаметр; 6 — измерительная диафрагма; 7 — смеситель; 8 — подача водопроводной воды; 9 — слив в канализацию; 10 — эжектор, создающий разряжение в хлораторе; 11 — отвод хлорной воды.
Воду можно обеззараживать и с помощью гипохлорита натрия, получаемого электролитическим способом (в электролизерах) на месте применения путем разложения раствора поваренной соли постоянным электрическим током.
Озонирование воды основано на применении озона, который легко разлагается с образованием атомарного кислорода, являющегося одним из наиболее сильных окислителей. Он уничтожает бактерии, споры, вирусы, обесцвечивает и дезодорирует воду, окисляя органические загрязнения.
Озон не изменяет природные свойства воды, так как его избыток быстро разлагается, превращаясь в кислород.
Озон получают из атмосферного воздуха в аппаратах, называемых озонаторами. Предварительно осушенный, очищенный и охлажденный воздух поступает в озонатор, в котором происходит разряд коронного типа, в результате чего образуется озон. Доза озона принимается при введении его в фильтрованную воду с целью обеззараживания 1—3 мг/л, а для подземной воды, не требующей очистки, 0,75—1 мг/л.
Обеззараживание воды можно проводить путем ее обработки ультрфиоле-товыми лучами. Обеззараживание воды бактерицидными лучами имеет преимущества перед хлорированием, так как природные вкусовые качества и химические свойства воды не изменяются. Бактерицидное действие лучей протекает во много раз быстрее, чем хлора; после облучения воду сразу можно подавать потребителям. Бактерицидные лучи уничтожают не только вегетативные виды бактерий, но и спорообразу- ющие. Эксплуатация установок для обеззараживания воды бактерицидными лучами проще хлорного хозяйства.
Наибольшим бактерицидным эффектом обладают ультрафиолетовые лучи с длиной волны 200—295 мкм. Эту область ультрафиолетового излучения называют бактерицидной. Источниками бактерицидного излучения служат выпускаемые отечественной промышленностью аргонортутные лампы низкого давления и ртутно-кварцевые лампы высокого давления.
Недостатком рассматриваемого метода является невозможность оперативного контроля за эффектом обеззараживания в отличие от хлорирования (по остаточному хлору).
ЛИТЕРАТУРА
1. Современные технологии подготовки воды для систем горячего водоснабжения (ГВС). Доклад к семинару «Современные материалы и технологии реконструкции цехов химводоподготовки котельной» 3 ноября 2005 г. в г. Нефтегорск Самарской области.
2. Сомов М.А., Квитка Л.А. «Водоснабжение» - ИНФРА-М, 2007. Раздел 5. Водоподготовка.
3. Статья из журнала «Водоснабжение и санитарная техника», 2012, №1
«Очистка геотермальных систем отопления и горячего водоснабжения от карбонаных отложений», к.т.н., старший научный сотрудник «Института Проблем Геотермии Дегестанского Научного Центра РАН» - Г.Я. Ахмедов.














 (zip - application/zip)
(zip - application/zip)